作為一種新興的腫瘤特異性治療手段�����,化學(xué)動力學(xué)治療(CDT)利用腫瘤內(nèi)的原位催化化學(xué)反應(yīng)誘導(dǎo)癌細胞的破壞���,在生物醫(yī)學(xué)領(lǐng)域引起了越來越多的關(guān)注����。通過鐵介導(dǎo)的Fenton或類Fenton反應(yīng)在特定的酸性腫瘤微環(huán)境中�����,CDT能有效地將腫瘤內(nèi)內(nèi)源性過量產(chǎn)生的活性氧(ROS)����、過氧化氫(H2O2)轉(zhuǎn)化為具有高度細胞毒性的羥基自由基(?OH)���,從而殺滅腫瘤細胞�。
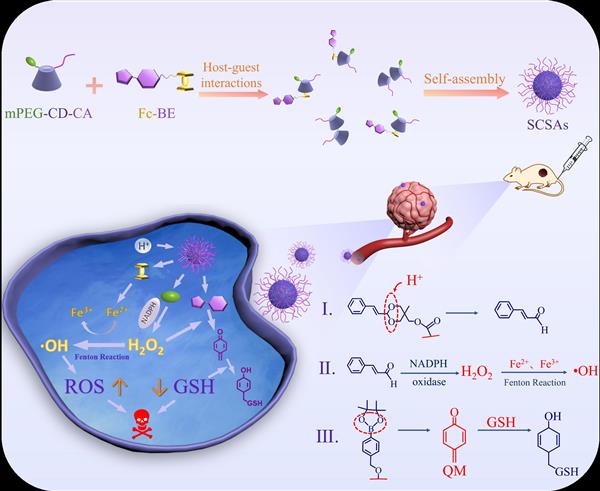
基于此,課題組設(shè)計了一個超分子自組裝體系,實現(xiàn)腫瘤特異性氧化應(yīng)激放大和級聯(lián)增強Fenton反應(yīng)的化學(xué)動力療法���。首先合成了一種由酸性敏感的縮醛鍵連接的肉桂醛和聚乙二醇修飾的β-環(huán)糊精(mPEG-β-CD-CA)。 然后���,F(xiàn)c部分與H2O2刺激響應(yīng)的苯硼酸頻哪醇酯(BE)結(jié)合合成Fc-BE。再利用Fc與β-CD之間的強主客體相互作用�,將疏水性的Fc-BE有效地包裹在親水性mPEG-CD-CA中����,形成兩親性超分子��,然后在水溶液中自組裝形成氧化還原刺激響應(yīng)的超分子自組裝體(SCSAs)�。超分子納米自組裝體通過腫瘤細胞的通透性和EPR效應(yīng)進入腫瘤細胞����,并富集在腫瘤組織內(nèi)�����。在腫瘤細胞酸性內(nèi)涵體/溶酶體環(huán)境下�����,觸發(fā)mPEG-CD-CA中的縮醛鍵斷裂,初步解離并釋放出CA���,游離CA激發(fā)胞內(nèi)NADPH氧化酶作用產(chǎn)生H2O2,而H2O2又通過二茂鐵的級聯(lián)Fenton反應(yīng)生成高細胞毒性的?OH�,提高細胞內(nèi)氧化水平�,增強細胞殺傷作用��;另一方面���,H2O2又與苯硼酸頻哪醇酯作用��,產(chǎn)生醌甲基自由基(QM)從而消耗腫瘤細胞內(nèi)的還原型谷胱甘肽(GSH)����,降低細胞內(nèi)還原水平�,從而協(xié)同放大CDT的療效。細胞實驗結(jié)果表明,該超分子自組裝體具有良好的癌細胞特異性殺傷效果����,在治療癌癥領(lǐng)域具有潛在的應(yīng)用價值��。研究成果最近被Chinese Chemical Letters接收(IF:6.779)