������ͨ��W���m/�R�������ڈF��_�l��һ�N����Ƕ��3D��ӡ���ԣ��ɹ����F�ˌ����y�����y�Լӹ��ğ���ԏ����w�����۹�����������PGS���ĸ߾��ȡ����������졣����ԓ�������F��c�����ֽ��ں������Ƴ��c���K���������N�ϵČ�늏����aƬ��ԓ�aƬ���H��ģ�M�ļ������W�����ԣ������ļ���������ģ����չ�F��Խ���ί�Ч����ͨ�^�ṩ�Cе֧�Ρ����̖���������MѪ�������c�����{������Ч���������K���ܣ���o�������K�aƬ���_�l�ṩ����˼·��
�о������c����˼·
�ļ������������ļ�����������pʧ�����Ҳ����ؘ�����������K�aƬ��Ҫ�߂��cԭ���ļ���ƥ������g���ԡ����Գ��܄ӑB׃�ε�ƣ�ڏ��ȡ����M���̖ͬ�������Č���ԣ��Լ��c���ұ�����s���ʹ��ε����S�νY�����۹�����������PGS�����䃞���ď����w�����������Զ��ɞ�������ϣ�������еĽ^�������Լ����s�Ă��y��̻���ˇ�����A����ճ�ȵ͡�ȱ���Y�������ԣ�����Ҫ�L�r�g�ߜ���ս�����ʹ�ìF��3D��ӡ���g�y��ֱ�������ͬ�r�M�����W��늌W�͎ΌWҪ���PGS�aƬ��ᘌ��@һ���𣬱��о������һ�N����Ƕ��ʽ��ӡ�²��ԣ����ÿ��{��׃���Ե�֧�λ��|���ڴ�ӡ�^���О�PGS�A���:�z�ṩ�R�r֧�Σ��Ķ����F�߱���D����ԭλ��̻�����ֱ�����칦�ܼ��ɵČ�늏����w�aƬ�_������;����
2025��10��30�գ����PՓ������Melt-Based Embedded Printing of Macroscopically-Conformal, Electro-Conductive and Elastomeric Patches for Improved Myocardial Infarction Repair�����}�l����Advanced Materials�ڿ��ϡ�
��l�F
��1�����gͻ�ƣ����F����PGS��Ƕ��ʽ��ӡ
�о��F����ß᷀����֧�λ��|���ɹ����F������PGS�ķ�����ӡ������ϵ�y�о���PGS�A�������׃���ԣ���ͨ�^�{�ػ��|�����������˷��˼��z�����y�}�����F���B�m�������PGS���z��ӡ���Mһ��������ӡ�����Ɍ���ӡ�ֱ������������e������С�����ߴ��c�����������Pϵ���Ͻ�������w����������Փ����ӡ���̻����PGS���z����⻬���������ܣ�չ�F�����õĎα���ȡ�
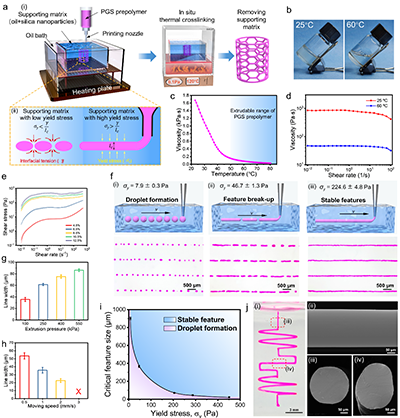
�D1. ����Ƕ��ʽ��ӡ�����cPGS�߾��ȳ���
��2���Y�����̣����W���ܿ��{�ď��s���S�Y��
ԓ��ӡ���������������⻬�����z�g�o�p�ںϵ�PGS�Y������ӡ��PGS��Ʒչ�F�������ď��ԣ����ё�׃���^500%��ͨ�^���_����ԭλ��̻��r�g�����ڌ��������`���{���䏗��ģ�������W���ܡ����⣬ԓ����߀�ɹ���ӡ���������Ľ��������ҿ������Ͷ��ӷ�C֧���ڃȵĸ��N���s���S�Y�������չʾ������������s���Π��ď���������
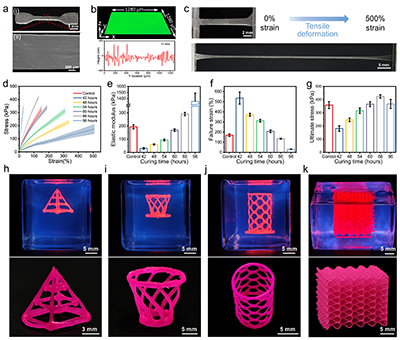
�D2. ��ӡ�Y�������W�����{���c���s���S����
��3�����ܼ��ɣ������N��������Č���aƬ
�F�ͨ�^���r��֦��̼�{��������PGS�Ǽܣ���Q���F�ۺʹ�ӡ�������y�}���Ƃ��˷�ɢ���ɴ�ӡ��PGS-CNT��늏ͺϲ��ϡ��S��CNT�������ӣ��ͺϲ����ڱ��ָߏ��Ե�ͬ�r��ģ����늌����@���������ҽ������ʿɿء����ڴ������K�����Sģ�ͣ��F��OӋ����ӡ���������m���Č�����K�aƬ��ͨ�^����Ԫ����������C�Y��������ʹ�aƬ�ڙM/�v�����ϳʬF���c��Ȼ�ļ���ƥ������W�����ԡ�

�D3. ���PGS-CNT�ͺϲ����Ƃ��c�������K�aƬ�OӋ
��4���w����C������aƬ���M�ļ����������cͬ������
�w�⼚�����������c��PGS��ȣ���PGS-CNT����aƬ�ϵ��ļ������������и����R���g϶�B�ӵ��ױ��_���ߣ��������P�����@�����{������Ҫ���ǣ�PGS-CNT�aƬ�ϵ��ļ��������F��ͬ����Ҏ�ɵ��}˲׃���ߵ��l�����l�ʣ������ܸ��õ�푑��ⲿ늴̼����C���ˌ�늾W�j���ļ���������ܳ�����@�����M���á�
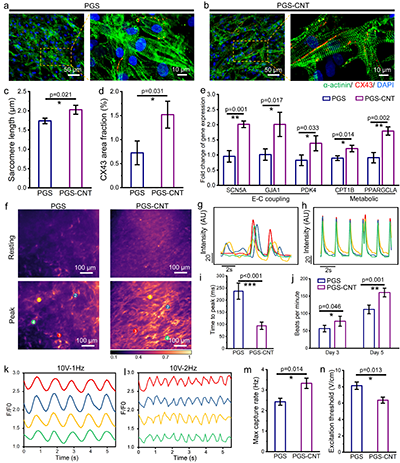
�D4. ����aƬ���M�ļ����������c�ͬ����
��5���w���ί�������aƬ��Ч�֏����K����
�ڴ����ļ�����ģ���У�ֲ��o������PGS-CNT����aƬ�������K���ܵõ��@�����ƺͻ֏͡����ĄӈD�@ʾ��PGS-CNT�M����Ч��ֹ���ҔU�������@���S���^�ߵ���������Ѫ�֔������w�^���@ʾ�aƬ�c���K�N�����ã��M����Ƭ�����Mһ���C����PGS-CNT�M������e��С�������^���ұ������Ч�������ļ������IJ����Էʴ�

�D5. ����aƬ��Ч�֏��ļ�����������K����
��6���fͬ�ޏͣ����MѪ�������c�{�������h��
������о���ʾ���aƬ���M�ޏ͵ąfͬ�C�ơ�ֲ���PGS-CNT�aƬ�@�����M�˹����^���Ѫ�����ɣ��e���γ��˸����������}��ͬ�r������aƬ���õر��o�˹����^��ȴ����ļ��M������������{�������߷�������ʹ���ɼ����Ĵ���M1������ޏ͵�M2�͘O���������K�ޏ̈́������������h����
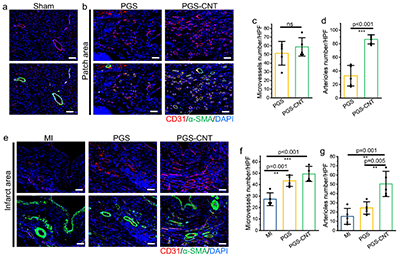
�D6. �aƬֲ����M�����^�Ĺ���Ѫ������

�D7. �aƬ�����ļ����沢�{�������h��
���Yչ��
���о��lչ��һ�Nͨ�õ�����Ƕ���ӡ���ԣ������˟���ԏ����w�߾���3D��ӡ���y�}�����ɹ��������Ƃ伯���ʽY��ƥ�䡢���W������ģ�M�c늌��ʼ�����һ�w�ĸ����ܟo�������K�aƬ���@�N�aƬͨ�^�Cе֧�Ρ�늂�������Ѫ�ܻ��������{���Ķ��fͬ���ã����F�ˌ��ļ���������Ч�ޏͣ�չ�F�˾���R���D��������
Փ���}Ŀ��Melt-Based Embedded Printing of Macroscopically-Conformal, Electro-Conductive and Elastomeric Patches for Improved Myocardial Infarction Repair
ԭ��朽ӣ�https://advanced.onlinelibrary.wiley.com/doi/abs/10.1002/adma.202512137
- ���X���Ҍ���Ҳ��i�w�о��T�Fꠡ�Matter��: ��Q�����w��ģ������չ�ԵĴ������L 2021-12-27
- �|�A��W���������ڈF�AFM�����F����ԏ����w�Ҝ��¿ɿ��ܽ���� 2021-09-22
- �пƴ�/���������dz����пƴ���� Adv. Mater.��3D��ӡ���D���~ - ���ܺ����F�������F���F�������� 2026-02-02
- ������/���ƴ�Ժ����ƽ�����������ı� Small�����ڶ�ܹ����l���Ŀ��ή���̻�3D��ӡ���� 2026-01-19
- ����������ˇ�w�S��W�컴�ЈF� AFM���߾���3D��ӡ�Ƃ�ɽ����t����е 2026-01-04
- �Ϸ��t�ƴ�W��С�ҽ��� ACS Nano���b�d�^�����@�ļ{���w��ͨ�^���ɺ�mTORͨ·��������Ĥ��Ƥ-�g�|�D�����M�Ĺ��ޏ� 2023-10-07
